靶向RNA测序在融合基因检测中的应用

融合基因是由染色体倒位、缺失和/或易位等基因组重排而发生的结构变异。基因融合可能与致癌特性相关,并可在多种癌症类型中驱动肿瘤发生。基因融合对于癌症诊断和治疗的重要性已得到广泛认可,包括血液系统恶性肿瘤和实体瘤。临床上使用多种技术来检测基因融合,包括逆转录聚合酶链反应(RT-PCR),使用融合探针或分离探针的荧光原位杂交 (Fluorescence in situ hybridization, FISH) 法等。前者检测转录本的前提是断点信息已知且目标位置集中在可扩增的区域内;后者则饱受复杂重排的挑战。
二代测序(Next-generation sequencing, NGS)能够在单个实验中评估大量潜在的融合。基于靶向DNA测序技术的大panel,通常覆盖多基因的全外显子、局部内含子与部分启动子,能够有效地检出包含致癌融合在内的多种变异类型1。对常见或已知融合发生区铺设探针并进行杂交捕获可检测许多常见的激酶融合,包括涉及BRAF、ALK、RET和ROS1的融合,以及MET外显子14跳跃突变。然而,这种基于DNA检测基因融合的方法存在诸多技术限制。图1列出基于DNA层面的分析可能导致融合检测假阴性的原因。以NTRK3融合检测为例,覆盖其内含子并非有效方式,因其涉及基因组断点的内含子13和14分别跨越93kb和92Kb。铺设如此大的内含子将导致整体panel显著扩大,带来成本增加及检测灵敏度下降。其他原因还包括:内含子高度重复序列比对困难带来了检测盲点;RNA测序在肿瘤细胞占比低的情况下仍然可以检测到高表达事件,DNA层面则影响较大;复杂的基因组重排导致序列比对或分析困难2。
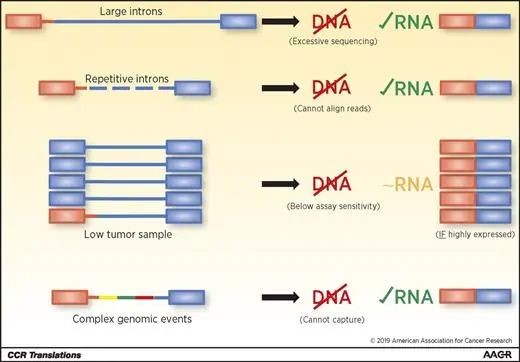
图1. 基因组复杂性或肿瘤丰度影响靶向测序融合检测的示意图2
靶向RNA测序专注于感兴趣的基因序列(图2),为转录本检测和定量提供高灵敏度分析。在实体瘤基因融合检测中,靶向RNA测序相比传统方法(FISH或RT-PCR)对融合基因诊断率有显著提升。近期的两项研究中该数值分别提升了13%3和22%4;在另一项儿童肉瘤的研究中,对RT-PCR融合基因测试呈阴性的样本进行测序分析,发现靶向RNA测序的结果可能影响其中27.8%病例的临床管理,包括化疗方案的改变,手术切除优于化疗,或整合靶向治疗5。靶向RNA测序的另一个优势是通过探针/引物设计可检测到新型融合基因6,7,从而增加融合基因的检测范围——包括罕见的融合基因和新的基因伴侣。鉴于这些优势,靶向RNA测序越来越多地用于融合基因的检测与分析。由于NTRK系列基因区域的复杂性,靶向RNA测序已被认为是鉴定NTRK融合的金标准8。
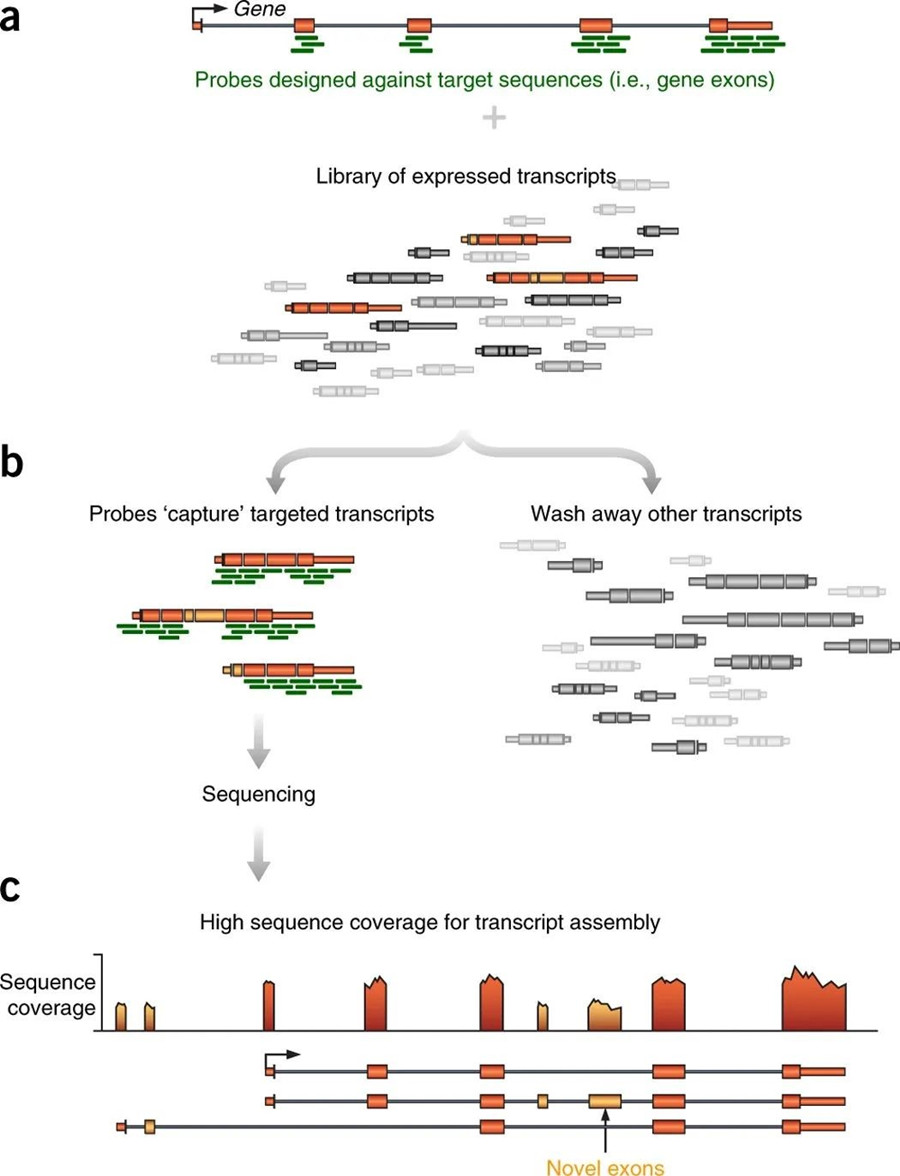
图2. 靶向RNA测序的常见流程9
(a)针对目标基因的外显子区铺设寡核苷酸探针。(b) 探针杂交并富集感兴趣的目标基因或区域。(c) 深度测序实现转录本组装、表达量化和新转录本(或融合)的灵敏检测。
仅使用靶向DNA测序分析融合的另一个缺点是,当检测到新的结构变异时,较难确定此类事件是否会导致功能性表达10。结合靶向DNA和RNA测序的综合型基因组分析(图3)可互为补充,有效检测并验证所有类型的基因组改变,包括融合转录本。该方法在血液肿瘤中已被证明可识别存在于低至10~20%细胞中的融合转录本,并展示了染色体重排导致的框内融合转录本的功能与表达11。实体瘤样本进行DNA和RNA同步NGS分析时,≥50ng DNA(≥3.3 ng/μl)和≥50ng RNA(最少7个拷贝/ng)的样本投入量及≥10%的肿瘤细胞含量对高灵敏度检测来说是必要的12。靶向RNA测序对DNA层面的补充作用在另一项2,522例肺腺癌患者的队列分析中得以证实:研究者发现靶向DNA测序呈驱动变异阴性的患者有33例从RNA分析中发现了基因重排,且融合阳性在低肿瘤突变负荷(tumor mutation burden, TMB)的阴性患者中相对富集13。
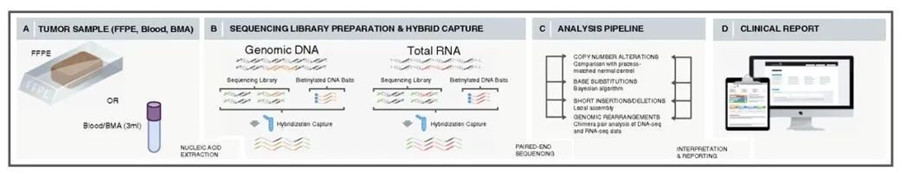
图3. 结合靶向DNA和RNA测序的综合型基因组分析
的工作流程14
肿瘤分子谱分析是精准肿瘤学的一个基本组成部分,其目的是识别基因和通路中的基因组变异,从而寻求临床“可及性”——治疗靶点或干预手段。靶向RNA测序,无论其本身用于融合检测,还是作为靶向DNA测序的补充,均可协助识别更多具有治疗意义的临床相关变异。
罗氏融合基因靶向RNA测序
完整解决方案
罗氏为不同样本类型和应用提供从样本到上机文库的全套靶向RNA测序解决方案,通过简化步骤提高工作效率,从源头把控测序数据质量,充分发挥每一份珍贵样本的临床价值。
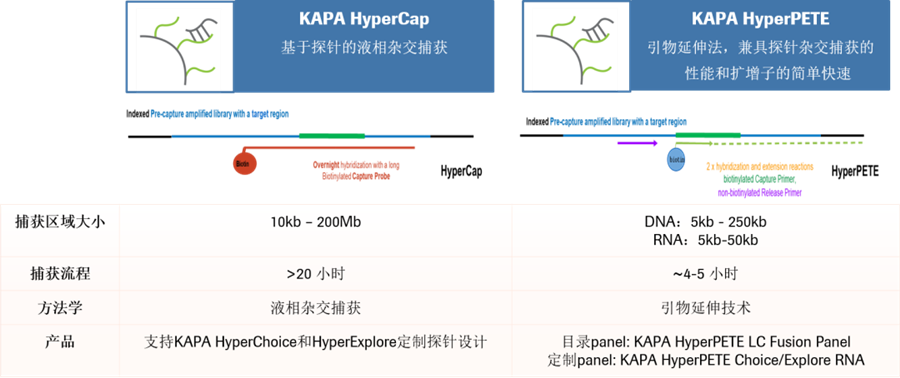
图4. 罗氏靶向RNA测序方案
图片来源:罗氏诊断整理
KAPA RNA Hyper文库构建产品特点:
单管反应,流程简化
微量、低质量样本建库性能卓越
扩增效率高、转录本覆盖度均一
PCR重复度低
高性能靶向建库,放大靶向信号,有利于分析低丰度融合转录本
RNA靶向富集方案
KAPA靶向富集panel设计采用罗氏经典算法,轻松覆盖复杂区域;行业领先的捕获均一性,有效降低测序成本;配套全流程实验方案,无需反复优化。罗氏既可以提供基于经典杂交捕获技术的KAPA HyperCap系列靶向捕获方案,又可以提供基于创新引物延伸技术的KAPA HyperPETE系列靶向捕获方案,满足临床多种应用需求。
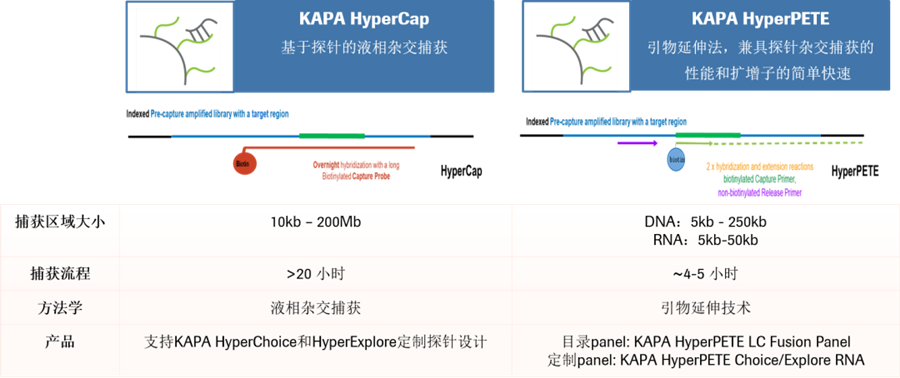
图5. 罗氏RNA靶向富集方案
图片来源:罗氏诊断整理
- 上一篇:没有了; 2023-03-03
- 下一篇:超声波清洗机超声波清洗器维修保养要点 2023-03-03

